自輔助生殖技術(ART)發展初期開始,未成熟卵母細胞的體外成熟(IVM)便被用於研究與臨床目的。
卵母細胞的成熟是一個高度專一的過程,依賴生殖細胞(卵子細胞)與體細胞(如卵丘細胞)之間複雜的互動關係。這種細胞間關係的複雜性,使得在體外成功實現卵母細胞成熟的探索過程極為艱鉅。
傳統的 IVM 是指在極輕度或無卵巢刺激的情況下,收集保留卵丘細胞包裹的完整卵母細胞進行培養。這種作法不再被視為實驗性,且被提出作為對多囊性卵巢或多囊性卵巢症候群患者更友善的治療選擇。相對地,補救性體外成熟(rescue-IVM,r-IVM)則是指從常規刺激週期中收集未成熟卵子後再行體外成熟的作法。這是一種實驗性程序,目的是解決部分患者卵子成熟率偏低的問題。
然而,實現有效的 r-IVM 更為困難,因為這些卵子是在去除卵丘細胞後才開始培養,因此缺乏來自體細胞的代謝與調節支持,而這些支持對卵子的成熟極為重要。停留在生發囊期(GV)或第一次減數分裂中期(MI)的卵子,在體外成熟的管理策略不同,且其後續發育與染色體正常性也不同。因此,若要將這些卵子用於臨床治療,必須採取量身定做的處理方式。
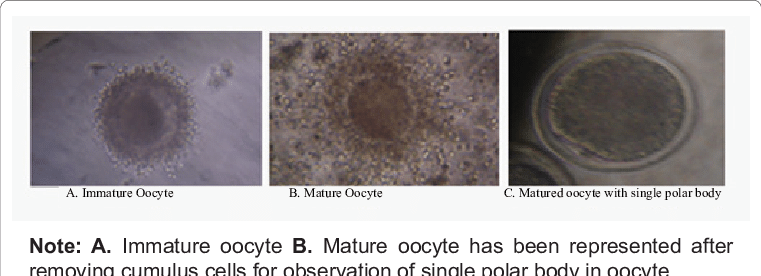
整體而言,由於未成熟卵子的成熟率與發育能力有限,r-IVM 的臨床效益也受到限制。這就引發了一個成本與效益的評估問題:即-如何界定 r-IVM 的適應症。在成熟卵子數量已經足夠的治療週期中,r-IVM 可能沒有實質意義。但對於特定預後不良的患者族群,如卵子成熟率低、可用卵子數少或卵子品質不佳的情況下,即便僅能額外取得一顆可用胚胎,都可能對治療結果產生幫助。
未來在此領域的進展,將取決於我們是否有能力在體外重現卵丘細胞對卵母細胞的核成熟與細胞質成熟所提供的支持機制。



